AG Wiedmann
Die Arbeitsgruppe für Translationale Präzisionsrhythmologie (AG Wiedmann) verfolgt das Ziel, die mechanistischen Grundlagen atrialer und ventrikulärer Kardiomyopathien durch einen integrierten Systemansatz besser verstehen zu lernen, der klinische Datenanalysen, zelluläre Elektrophysiologie, Multi-Omics-Profile, Großtiermodelle und computergestützte Modellierung umfasst. Übergeordnetes Ziel ist es, die Mechanismen die zu kardialer Dysfunktion, Arrhythmogenese und zerebraler Beeinträchtigung beitragen zu definieren und diese Erkenntnisse in präzisionsmedizinische Therapieansätze, device-basierte Interventionen und klinisch einsetzbare Biomarker zu überführen.
Im Zentrum des Forschungsprogramms steht die atriale Kardiomyopathie, die nicht nur als Substrat für Vorhofflimmern und die Herzinsuffizienz mit erhaltener Ejektionsfraktion (HFpEF), sondern auch als relevanter Faktor für den kognitiven Abbau betrachtet wird. Die zugrunde liegenden Krankheitsmechanismen sollen über verschiedene biologische Ebenen hinweg untersucht werden: von Ionenkanal-Remodelling, Transkriptionsfaktor-Dysregulation, epigenetischer Regulation, gestörter mechano-elektrischer Kopplung und fibrotischem Umbau bis hin zu Veränderungen der zerebralen Perfusion, des metabolischen Signalings und neuroinflammatorischer Prozesse. Die experimentelle Basis umfasst klinische Datensätze, humanes Vorhofgewebe, iPSC-dervied Kardiomyozyten sowie klinisch relevante Großtiermodelle und bietet damit eine robuste translationale Plattform.
Ein besonderes Merkmal des Labors ist die Integration von computergestützter und experimenteller Kardiologie. Hochdimensionale Daten aus Single-Nuclei RNA-Sequenzierung, Proteomik und automatisierter Patch-Clamp-Elektrophysiologie werden durch systembiologische Analysepipelines für Netzwerkanalysen, in silico Wirkstoffscreening und Target-Validierung verarbeitet. Diese Werkzeuge beschleunigen die Hypothesengenerierung und ermöglichen die Rückübersetzung klinischer Beobachtungen in mechanistische Modelle.
Zur direkten klinischen Translation betreibt das Labor ein spezialisiertes elektrophysiologisches Großtierprogramm. In Modellen des burst-pacing-induzierten Vorhofflimmerns und pTAC-basierten HFpEF-Schweinemodellen (perkutan, stentbasiert) werden Gentherapien, Schrittmacheralgorithmen und antiarrhythmische Substanzen mithilfe modernster interventioneller Bildgebung und high-density elektroanatomsichen Mapping-Technologien evaluiert. Diese Modelle dienen zugleich der Untersuchung der kardio-neuronalen Kopplung in vivo und ermöglichen die Analyse, wie atriale Dysfunktion und reduziertes Herzzeitvolumen die zerebrale Perfusion, neuronale Aktivität und funktionelle Konnektivität des Gehirns beeinflussen.

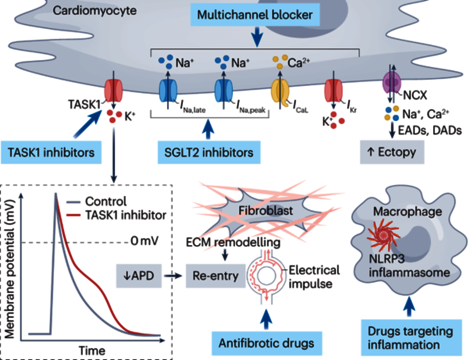
Diese experimentellen Modelle sind in eine translationale Pipeline eingebettet, die durch die lokale DZHK-Infrastruktur unterstützt wird und eine schnelle Überführung mechanistischer Erkenntnisse in die klinische Anwendung ermöglicht. Mechanistische Beobachtungen können retrospektiv in Patientenkohorten validiert und in frühe prospektive klinische Studien überführt werden.
Ein zentrales translationales Ziel ist die Entwicklung digitaler Biomarker zur Verbesserung der Risikoprädiktion, Patientenselektion und Therapieoptimierung. KI-gestützte EKG-Analysen, zirkulierende RNA-Marker und elektrophysiologische Mapping-Signaturen werden hierfür integriert, um prädiktive Modelle zur Risikostratifizierung, Arrhythmie-Rezidivwahrscheinlichkeit, Krankheitsprogression und Therapieansprechrate zu generieren.
Diese systemische Perspektive reflektiert die zentrale Hypothese des Labors: Herzrhythmusstörungen entstehen aus dem Zusammenspiel molekularer, metabolischer, struktureller und neuronaler Faktoren.
Durch die Verbindung mechanistischer Entdeckung mit computergestützter Vorhersage und translationaler Validierung verfolgt das Labor das Ziel, ein neues Paradigma der Systemkardiologie zu etablieren: mechanistisch präzise, digital integriert und klinisch umsetzbar. Die langfristige Vision ist die Entwicklung personalisierter Therapien, die das Fortschreiten von Vorhofflimmern verhindern, kardiales Remodeling rückgängig machen und die kognitive Funktion bei Patientinnen und Patienten mit Kardiomyopathien erhalten.
Kooperationen
Kontakt

Kontaktinformationen
- Telefon: +49 551 3968880
- E-Mail-Adresse: felix.wiedmann(at)med.uni-goettingen.de
Facharzt für Innere Medizin und Kardiologie
Zusatzqualifikation Spezielle Rhythmologie (Invasive Elektrophysiologie und Aktive Herzrhythmusimplantate)FESC (Fellow of the ESC)
FEHRA (Fellow of the European Heart Rhythm Association)
